كلورات
من دار الحكمة
اذهب إلى التنقلاذهب الى البحث
| كلورات | |
|---|---|
| الخواص | |
| الصيغة الجزيئية | ClO₃⁻ |
| المعرفات | |
| CAS | 14866-68-3 |
| بوب كيم | 104770[1] |
|
|
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
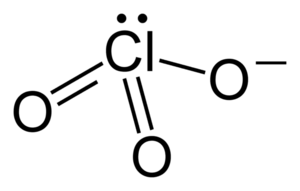
أيون الكلورات هو أيون سالب له الصيغة −ClO3.[3][4][5] تسمى المركبات الكيميائية التي تحوي هذا الأيون أيضاً بالكلورات، وهي مشتقة من حمض الكلوريك. من الأمثلة على أملاح الكلورات مركب كلورات البوتاسيوم KClO3 وكلورات الصوديوم NaClO3.
التحضير
تحضر أملاح الكلورات القلوية من تمرير غاز الكلور في المحلول القلوي الموافق، كما هو الحال مع كلورات البوتاسيوم:
أما أملاح الكلورات الأخرى مثل كلورات الفضة فتستحصل من نظيراتها القلوية.
الخواص
يكون عدد أكسدة الكلور في هذه الأملاح +5، بالتالي فهي تتمتع بخواص مؤكسدة جيدة.
توجد هناك صيغ رنينية مختلفة لهذا الأيون:

الاستخدامات
نظراً لخطورتها فإن مركبات الكلورات عموماً ذات تطبيقات عملية قليلة.
مراجع
- ↑ 1٫0 1٫1 1٫2 1٫3 14866-68-3 (بEnglish), QID:Q278487
- ↑ ChEBI release 2020-09-01، 17 أبريل 2025، QID:Q98915402
- ↑ Rao، B.؛ Hatzinger، P. B.؛ Böhlke، J. K.؛ Sturchio، N. C.؛ Andraski، B. J.؛ Eckardt، F. D.؛ Jackson، W. (2010). "Natural Chlorate in the Environment: Application of a New IC-ESI/MS/MS Method with a Cl18O3− Internal Standard". Environ. Sci. Technol. ج. 44: 8429–8434. Bibcode:2010EnST...44.8429R. DOI:10.1021/es1024228. PMID:20968289.
- ↑ J. Danielsen؛ A. Hazell؛ F. K. Larsen (1981). "The structure of potassium chlorate at 77 and 298 K". Acta Crystallogr. B. ج. 37: 913–915. DOI:10.1107/S0567740881004573.
- ↑ Coates، J. D.؛ Achenbach، L. A. (2004). "Microbial perchlorate reduction: rocket-fuelled metabolism". Nature Reviews Microbiology. ج. 2 ع. July: 569–580. DOI:10.1038/nrmicro926. PMID:15197392.
في كومنز صور وملفات عن Chlorate ion.